1. Czy chlor zmniejsza BZT?
Podsumowanie: Ten artykuł bada wpływ zawieszonych ciał stałych i materii organicznej na wydajność dezynfekcji chloru i UV Greywater. Badanie wykazało, że nawet niskie stężenia zawieszonych ciał stałych miało negatywny wpływ na dezynfekcję chloru, podczas gdy napromieniowanie UV nie miało wpływu na wyższe stężenia. Opracowano wiele modeli regresji liniowej w celu przewidywania wymagań dotyczących dawki chloru lub UV na podstawie początkowych stężeń zawieszonych ciał stałych, materii organicznej i wolnego chloru. W artykule omówiono także znaczenie leczenia Greywater do celów nie do przyczyny w celu złagodzenia wyczerpania zasobów wodnych i zmniejszenia kosztów.
Kluczowe punkty:
1. Ponowne wykorzystanie Greywater może obniżyć zużycie wody domowej.
2. Greywater musi być leczony i dezynfekowany ze względu na zdrowie użytkowników.
3. Chlorowanie i napromienianie UV są powszechnie stosowane metody dezynfekcji.
4. Chlor jest skuteczny i opłacalny, ale toksyczny i żrący.
5. Napromieniowanie UV uszkadza mikroorganizmy poprzez reakcje fotochemiczne.
6. Skuteczność dezynfekcji można zmniejszyć przez cząstki cząstkowe i substancje organiczne.
7. Zapotrzebowanie na chlor wzrasta wraz z obecnością rozpuszczonej i zawieszonej materii organicznej.
8. Mikroorganizmy przymocowane do cząstek są mniej skutecznie dezynfekowane przez chlor.
9. Materia organiczna może stabilizować błony komórkowe drobnoustrojów, zmniejszając wydajność chloru.
10. Materia organiczna może prowadzić do tworzenia produktów ubocznych dezynfekcji.
11. Cząstki cząstkowe zmniejsza dawkę UV otrzymywaną przez mikroorganizmy, zmniejszając wydajność.
12. Obecność cząstek i organicznych w Greywater jest powszechna.
13. Zaleca się usuwanie materii organicznej przed chlorowaniem.
14. Wpływ cząstek stałych i organicznych na wydajność dezynfekcji UV jest mniej badana.
15. Dezynfekcja UV jest opłacalna i nie wymaga dodatków chemicznych.
Pytania:
1. W jaki sposób ponowne wykorzystanie zużycia wody w Greywater jest?
Odpowiedź: Ponowne wykorzystanie szarości zmniejsza zużycie wody domowej, łagodząc presję na wyczerpane zasoby wodne i zmniejszając koszty wody gospodarstwa domowego.
2. Jakie są dwa powszechnie stosowane metody dezynfekcji dla Greywater?
Odpowiedź: Dwie powszechnie stosowane metody dezynfekcji wód szarości to chlorowanie i napromienianie UV o niskim ciśnieniu.
3. Co sprawia, że chlor jest opłacalnym środkiem dezynfekującym?
Odpowiedź: Chlor jest uważany za opłacalny, ponieważ jest skuteczny w stosunku do szerokiego spektrum patogenów i pozostałości chloru resztkowego w ścieku, zapewniając ciągłe dezynfekcję w całym systemie transportu.
4. Jakie są zalety napromieniowania UV o niskim ciśnieniu?
Odpowiedź: Napromieniowanie UV o niskim ciśnieniu nie wymaga dodatków chemicznych, jest skuteczne na licznych patogenach, opłacalnych, i ma prostą i bezpieczną eksploatację i konserwację.
5. Jak obecność cząstek stałych i substancji organicznych wpływa na dezynfekcję chloru?
Odpowiedź: Obecność cząstek stałych i substancji organicznych zwiększa zapotrzebowanie na chlor i zmniejsza ogólną wydajność dezynfekcji. Mikroorganizmy przymocowane do cząstek są mniej skutecznie dezynfekowane przez chlor, a materia organiczna może stabilizować błony komórkowe drobnoustrojów, co dodatkowo zmniejszając wydajność chloru.
6. Jakie są potencjalne zagrożenia związane z materią organiczną w procesie dezynfekcji?
Odpowiedź: Materia organiczna może prowadzić do tworzenia produktów ubocznych dezynfekcji, z których niektóre są znane lub podejrzane rak.
7. W jaki sposób cząstki cząstkowe wpływają na wydajność dezynfekcji UV?
Odpowiedź: Cząstki cząstkowe zakłóca ekspozycję mikroorganizmów na napromieniowanie UV poprzez ich ochronę, wchłaniając lub rozpraszając światło, zmniejszając dawkę UV otrzymywaną przez mikroorganizmy, a następnie zmniejszając wydajność dezynfekcji UV.
8. Dlaczego zaleca się usuwanie materii organicznej przed chlorowaniem?
Odpowiedź: Usunięcie materii organicznej przed chlorowaniem zmniejsza zapotrzebowanie na chlor i potencjał odrastania drobnoustrojów, poprawiając wydajność dezynfekcji.
9. Jakie limity zostały zaproponowane dla zawieszonych ciał stałych w Greywater?
Odpowiedź: Artykuł nie wspomina o konkretnych limitach dla zawieszonych ciał stałych w Greywater.
10. W jaki sposób modele regresji mogą pomóc przewidzieć wymagania dotyczące dawki chloru lub UV?
Odpowiedź: Modele regresji opracowane w badaniu mogą ustalić korelacje między początkowymi stężeniami zawieszonych ciał stałych, materią organiczną, wolnym chlorem i wydajnością dezynfekcji. Modele te można wykorzystać do przewidywania wymaganego resztkowego stężenia chloru lub dawki UV dla reaktorów przepływowych na miejscu.
11. Jakie korzyści oferuje leczenie Greywater do celów nie do zrobienia?
Odpowiedź: Traktowanie Greywater do celów nie do podkładu zmniejsza popyt na zasoby słodkowodne, co powoduje niższe koszty wody i łagodzenie wyczerpania zasobów wodnych.
12. Jakie są potencjalne ryzyko stosowania nietraktowanej Greywater?
Odpowiedź: Nietraktowana Greywater zawiera patogeny i inne zanieczyszczenia, stanowiąc zagrożenia dla środowiska i zdrowia, jeśli są stosowane bez leczenia i dezynfekcji.
13. Dlaczego przechowywanie, obsługa i zastosowanie chloru są ważne?
Odpowiedź: Chlor jest toksyczny i żrący, dlatego konieczne są odpowiednie przechowywanie, obsługa i zastosowanie, aby zapewnić bezpieczeństwo i zapobiegać wypadkom.
14. Jakie zalety oferują napromienianie UV niskociśnieniowe w małych systemach na miejscu?
Odpowiedź: Napromieniowanie UV o niskim ciśnieniu nie wymaga dodatków chemicznych, jest skuteczne w wielu patogenach, opłacalnych pod względem początkowej inwestycji kapitałowej i poziomów operacyjnych, a także proste i bezpieczne działanie i konserwacja.
15. W jaki sposób można rozwiązać wpływ cząstek stałych i organicznych na wydajność dezynfekcji?
Odpowiedź: Artykuł sugeruje usunięcie materii organicznej przed chlorowaniem i podkreśla potrzebę dalszych badań nad wpływem cząstek stałych i organicznych na wydajność dezynfekcji UV.
Czy chlor zmniejsza BZT?
Nasze systemy wykryły niezwykłą aktywność ruchu z Twojej sieci. Wypełnij tę Recaptcha, aby pokazać, że to ty składasz prośby, a nie robot. Jeśli masz problem z widzeniem lub wypełnieniem tego wyzwania, ta strona może pomóc. Jeśli nadal będziesz doświadczać problemów, możesz skontaktować się z wsparciem JSTOR.
Wpływ zawieszonych ciał stałych i materii organicznej na efektywność dezynfekcji chloru i UV w Greywater
Ponowne wykorzystanie Greywater (GW) może obniżyć zużycie wody domowej. Jednak GW musi być leczony i zdezynfekowany w celu zapewnienia zdrowia użytkownika. Badania badane w skali laboratoryjnej oraz w konfiguracjach przepływowych, które są ogólnie stosowane w leczeniu GW na pełną skalę, wydajność dezynfekcji dwóch powszechnie stosowanych technologii (a) Chlorowanie i (b) napromienianie UV o niskim ciśnieniu. Metody dezynfekcji badano w powszechnie znajdującym się zakresie całkowitego zawieszonych ciał stałych (TSS; 3.9–233 mg/l) i 5-D biochemiczne zapotrzebowanie na tlen (BZT5) Stężenia (0–107 mg/l) jako reprezentatywny/proxy biodostępnej materii organicznej. Negatywny wpływ TSS rozpoczął się nawet przy niskich stężeniach (5 Na inaktywacji FC zaobserwowano tylko wtedy, gdy jego stężenie było wyższe niż 50 mg/l. Wiele modeli regresji liniowej opracowano po wynikach laboratoryjnych, ustanawiając korelację między inaktywacją FC przez chlorowanie lub napromieniowanie UV a początkowym FC, TSS i BZT5 stężenia. Modele zostały zatwierdzone w stosunku do wyników reaktorów przepływowych i wyjaśniły większość zmienności mierzonej inaktywacji FC. Ustalono współczynniki konwersji między skalami laboratoryjnymi a eksperymentami reaktora przepływowego. Umożliwiają one przewidywanie wymaganego resztkowego stężenia chloru lub dawki UV potrzebnej do reaktora przepływowego na miejscu. Takie podejście jest cenne zarówno z perspektywy operacyjnej, jak i badawczej.
1. Wstęp
Greywater (GW; ścieki domowe z wyłączeniem wody toaletowej) ponowne wykorzystanie do celów bezpotowanych, takich jak nawadnianie ogrodu, może zmniejszyć zapotrzebowanie na wodę domową, a tym samym złagodzić presję na wyczerpane zasoby wodne, jednocześnie zmniejszając koszty wody gospodarstwa domowego [1]. Jednak nietraktowany GW zawiera patogeny i inne zanieczyszczenia i może stanowić zagrożenia dla środowiska i zdrowia, jeśli stosowane bez leczenia i dezynfekcji [2,3]. Chlorowanie i napromienianie UV o niskim ciśnieniu są prawdopodobnie najczęściej stosowanymi metodami dezynfekcji w małych systemach GW na miejscu [4,5,6].
Chlor jest niezawodnie skutecznie w stosunku do szerokiego spektrum patogennych mikroorganizmów i jest uważany za opłacalny środki dezynfekujące [3,7]. Ponadto resztkowy chlor pozostaje w ściekach po zastosowaniu, zapewniając dalsze dezynfekcję w całym systemie transportu, zmniejszając powrót potencjału [8,9]. Ponadto dawkowanie chloru jest elastyczne i może być kontrolowane przez proste, tanie urządzenia. Niemniej jednak chlor jest toksyczny i żrący; Zatem jego przechowywanie, wysyłka, obsługa i aplikacja muszą być zarządzane odpowiedzialnie.
Napromieniowanie UV zapobiega replikacji mikroorganizmów poprzez reakcje fotochemiczne, które uszkadzają ich kwasy nukleinowe w DNA lub RNA [10]. Główne przyczyny zastosowania niskociśnieniowego promieniowania UV (254 nm) w małych systemach na miejscu są: (1) Nie wymaga dodatków chemicznych (nieistotne dla chlorowania, przechowywania i dawkowania), (2) okazało się, że jest to skuteczne na licznych patogenach, w tym wirusach i pierwotkach, a pierwotnie, które stwierdzono, że są one opowiadanie o wartościach, a (4) zarówno w zakresie operacji, jak i (4). a konserwacja jest prosta i bezpieczna [4].
Należy zauważyć, że w instalacjach na pełną skalę zgłaszano różne skuteczność dezynfekcji [11], a niektóre badania wykazały, że jakość wody o wartości poniżej standardu może zmniejszyć wydajność zarówno dezynfekcji chloru, jak i UV. W szczególności obecność cząstek stałych i substancji organicznych w wodzie może negatywnie wpłynąć na te metody dezynfekcji’ Występy [4,12]. W przypadku chlorowania, ten negatywny efekt ulega ekspresji poprzez zwiększenie zapotrzebowania na chlor, ponieważ rozpuszczona i zawieszona materia organiczna jest utleniona przez chlor. Zatem ogólna wydajność dezynfekcji zmniejsza się. Mikroorganizmy przyczepiają się do cząstek obecnych w wodzie, zmniejszając w ten sposób szansę na skuteczny kontakt między mikroorganizmem a chlorem, w porównaniu z bakteriami niezaciągnymi [12,1 3]. Co więcej, obecność materii organicznej może dodatkowo zmniejszyć wydajność dezynfekcji chloru poprzez stabilizowanie błon komórkowych mikrobiologicznych [14]. Wreszcie obecność materii organicznej może prowadzić do tworzenia niechcianych produktów ubocznych dezynfekcji (w tym znanych lub podejrzanych rakotwórczych), tym samym nie tylko utrudniając proces dezynfekcji [15], ale także stanowi zagrożenie dla zdrowia zagrożenia dla zdrowia. Winward i in. [12] zbadali wpływ organicznego i cząstek stałych na dezynfekcję chloru GW w układzie wsadowym i twierdzili, że wzrost materii organicznej zwiększył zapotrzebowanie na chlor, ale nie wpłynęło na całkowitą liczbę coli’ Odporność na chlor. Jednak autorzy ci zalecili usunięcie materii organicznej przed chlorowaniem w celu zmniejszenia zapotrzebowania na chlor i potencjału odrastania drobnoustrojów.
W przypadku napromieniowania UV cząstki zakłócają ekspozycję docelowych mikroorganizmów na napromieniowanie [15,16,17], albo przez ich ochronę, albo przez wchłanianie lub rozpraszanie światła, zmniejszając w ten sposób dawkę UV otrzymaną przez mikroorganizmy’Skuteczność. Obecność cząstek stałych i organicznych w GW odnotowano w wielu badaniach, ale tylko nieliczni omówili ich niekorzystny wpływ na wydajność dezynfekcji UV. Na przykład autorzy [4] badali dezynfekcję sztucznego GW, proponowane limity 60 mg/l zawieszonych ciał stałych i zmętnienie 125 NTU, poza których GW nie można praktycznie zdenerwować w celu osiągnięcia 4-logowej redukcji bliliform z bali z baliliami (FC), niezależnie od wymiarów reaktora UV, niezależnie od wymiarów reaktora UV UV. Ref. [18] zalecił usunięcie cząstek przez filtrację w celu uzyskania poziomu zmętnienia 2 NTU (Nefelometryczne jednostki zmętnienia), aby zwiększyć wydajność dezynfekcji UV. Inne badania koncentrowały się na rozmiarach cząstek, które blokują mikroorganizmy ze światła UV [12] oraz na określonych typach cząstek związanych z niektórymi bakteriami w leczonych GW, które powodują ochronę bakteryjną przed dezynfekcją UV [19].
Co ciekawe, nie ma systematycznych informacji dotyczących połączonego wpływu zawieszonych ciał stałych i materii organicznej (mierzonej jako biochemiczne zapotrzebowanie na tlen 5-D (BZT (BZT (BZT5)), w przypadku niskociśnieniowego dezynfekcji UV i dezynfekcji chloru zarówno w jednostkach dezynfekcji wsadowej, jak i ciągłego przepływu. Badanie to miało na celu przetestowanie wydajności zarówno metod dezynfekcji na GW w zakresie całkowitej zawieszenia substancji stałych (TSS) i BZT5 stężenia. Eksperymenty przeprowadzono w kontrolowanych grupach laboratoryjnych i w reaktorach przepływowych. Ponadto badanie’Cele obejmowały opracowanie modeli regresji w celu przewidywania wpływu TSS i BZT5 na temat efektywności dezynfekcji chloru i UV w obu konfiguracjach.
2. Materiały i metody
Badania przeprowadzono w dwóch etapach. Początkowo traktowane próbki GW, zmieniające się w TSS i BOD5 Stężenia, dezynfekowano w konfiguracji partii przez roztwór podchlorynowy lub promieniowanie UV za pomocą kolimowanej wiązki. Wyniki uzyskane z tego etapu zastosowano do opracowania dwóch modeli regresji liniowej (jeden do chlorowania, a drugi do napromieniowania UV). W drugim etapie traktowany GW, z systemów obróbki na miejscu (przedstawiony pod spodem), został zdezynfekowany w jednostce dezynfekcji przepływowej przy użyciu jednej z dwóch metod: tabletki chloru lub komercyjnego UV niskociśnieniowego UV. Modele’ Zbadano możliwość zastosowania i weryfikację, a następnie porównano z wynikami drugiego etapu.
2.1. System leczenia GW
Do leczenia domowego GW zastosowano jedenaście jednoosobowych pełnometrażowych systemów recyrkulujących przepływu pionowego (RVFCW). System RVFCW zawierał dwa 500-letnia plastikowe pojemniki (1.0 m × 1.0 m × 0.5 m) umieszczone na sobie. Górny pojemnik, który miał perforowane dno, zawierało sadzone trójwarstwowe łóżko, podczas gdy dolny pojemnik działał jako zbiornik. Łóżko składało się z 10-cm dolnej warstwy wapiennych kamyków, z 35-cm środkowej warstwy żwiru tufu i 5-cm górnej warstwy drewna. GW został pompowany ze zbiornika równoznacznego z osadnictwem, z którego został przekazany na szczyt łóżka. Stamtąd przepłynęło przez warstwy łóżka (nienasycony przepływ) i do zbiornika. GW poddano recyrkulowaniu z zbiornika do górnego łóżka z prędkością około 300 l/h przez 8 godzin, po czym filtrowano go przez filtr 130 μm, a następnie ponownie wykorzystano do nawadniania ogrodu. Dodatkowe szczegóły dotyczące systemu można znaleźć w [20,21].
2.2. Eksperyment wsadowy
Traktowane domowe próbki GW (1 l) z 11 RVFCW zebrano co najmniej cztery razy wzdłuż badania i sprowadzono do laboratorium krótko po pobraniu w chłodnicy. Jakość leczonego GW poddano obróbce wstępnie pod kątem następujących parametrów: TSS metodą grawimetryczną, BZT5 Przy użyciu standardowych butelek o mocy 300 ml, % transmisji napromieniowania przy 254 nm przez spektrofotometr (Genesys 10, Thermo), zmętnienie za pomocą mętności HACH 2100P i FC metodami filtracji błony przy użyciu Agar MTEC (Lesher, Michigan USA, Atumedia). Wszystkie analizy były zgodne ze standardowymi procedurami [22].
Leczone próbki GW badano tak, jak IS lub po tym, jak zostały poddane wzrostowi stężenia w obu TSS (końcowe stężenia TSS w zakresie od 1–130 mg/l) lub materii organicznej (mierzone jako BZT BZT5 ze stężeniami w zakresie od 3–100 mg/l) lub połączeniem zarówno zawieszonych cząstek, jak i stężeń materii organicznej przy różnych stosunkach. Zwiększenie TSS przeprowadzono przez dodanie różnych ilości sproszkowanych wysuszonych substancji stałych do obróbki GW. Zawieszone ciała stałe przygotowano przez zatwierdzenie surowego GW (wirowanie przy 6000 rpm przez 5 minut) i susząc osad w 60 ° C przez 48 godzin. Stężenie materii organicznej zwiększyło się przez wprowadzenie różnych ilości 0.2 μM-filtrowane surowe GW ze znanym BOD5 stężenia do leczonych GW. Wymagane elementy mieszano w zlewce przez 15 minut, aby wytworzyć jednolitą mieszaninę. Dodatkowo FC wprowadzono przez dodanie < 0.5 mL/L GW sample of kitchen effluent to ensure FC concentrations of 10 4 to 10 5 CFU/100 mL. Overall, 432 combinations were tested.
Subsamples analizowano przed i po dezynfekcji, po ustaleniu wydajności dezynfekcji przez obliczenie logarytmicznej inaktywacji FC.
2.2.1. Eksperyment chlorowania
Skuteczne zastosowanie środka dezynfekcyjnego powinno wziąć pod uwagę wymaganą dawkę, którą można osiągnąć poprzez zmianę stężenia chloru i czasu kontaktu z dezynfekcją. Wymagana dawka różni się w zależności od zapotrzebowania na chlor (charakterystykę ścieków) i resztkowe wymagania chloru. Według [23] wolne resztkowe stężenie chloru powinno wynosić ≥0.5 mg/l po co najmniej 30 minutach kontaktu w pH < 8.0. Subsamples were disinfected in a batch mode. Initially, the chlorine demand of the subsamples was determined. For this, aliquots of 25 mL were exposed to four different chlorine doses of 0.5, 1, 3, and 6 mg/L. Samples were gently stirred and after 1 h, the total and free residual chlorine levels were determined by the DPD method [22].
2.2.2. Klimatyzowana konfiguracja wiązki
Quasi-równolegle urządzeń UV w skali wiązki (Trojan Technologies Inc., Ontario, Kanada) zastosowano do przetestowania wydajności dezynfekcji UV (rysunek S2). System składał się z 11-W niskociśnieniowej pary rtęci germicidal UV, emitując monochromatyczne promieniowanie UV przy 254 nm bezpośrednio nad wewnętrzną 25-cm nierefleksyjną wiązką z kolimowaną o średnicy 40 mm. Do pomiaru intensywności padającego światła UV zastosowano radiometr ILT 1700 (międzynarodowe światło, Peabody, Massachusetts, USA) z detektorem wrażliwym na 254 nm (IL Photonic SED240). Próbki (25 ml podwielokrotności) umieszczono pod rurką kolimacyjną w naczyniu krystalizacji 50 × 35 mm i zmieszano z mieszającym paskiem (~ 110 rpm), umożliwiając jednolite stosowanie dawki UV do całej próbki do całej próbki do całej próbki.
Kontrola dawki UV przeprowadzono za pomocą migawki, która pozwoliła na zmianę czasu ekspozycji próbki mieszanej. Próbki wystawiono na trzy dawki napromieniowania UV: 7.5, 15 i 30 MJ/cm 2 . Czasy ekspozycji dla każdej dawki UV zależały od kilku czynników, w tym: intensywności incydentu, odbicia, czynników Petriego, rozbieżności i czynników wodnych. Metody zastosowane do określania tych czynników opisano w [24]. Czynniki rozbieżności i odbicia były stałe we wszystkich eksperymentach, a ich wartości wynosiły 0.960 i 0.Odpowiednio 975. Współczynnik Petriego obliczono co tydzień i uśredniono 0.88 ± 0.05. Współczynnik wody wahał się od 0.40 do 0.89, a intensywność padania zmierzona na powierzchni wody wahała się od 0.30 do 0.32 MW/cm 2 .
2.3. Konfiguracje przepływowe
Leczone próbki GW (10 l) pobrano z pełnej jednorodzinowej rany RVFCW na miejscu (sekcja 2.1 powyżej), natychmiast przetransportowany do laboratorium i służył jako napływ do jednostek dezynfekcji przepływu ciągłego. Wszystkie próbki analizowano pod kątem TSS, BOD5, % transmisja napromieniowania przy 254 nm, zmętnienie i FC, jak opisano powyżej. Po dezynfekcji próbki ponownie analizowano dla FC.
2.3.1. Przetwana komora chlorowania
Chlorowanie przeprowadzono przez rozładowanie leczonych GW (przy z góry określonej prędkości przepływu) za pomocą komory 500 ml zawierającej tabletkę HTH o powolnym uwalnianiu (wysoko testowy hipochloryt; 70% dostępnego chloru, hydro-linia, Silinierby, Finlandia). Komora była obudową filtra AMIAD o 500 ml bez filtra (model. BSP 1 ″, Amiad Ltd., Amiad, Isael; Rysunek 1a). Pojedyncza tabletka chloru umieszczono w komorze przepływowej i została zaprojektowana do powoli rozpuszczania się, gdy woda przepływa przez komorę, zgodnie z określonym czasem kontaktu. Komora była połączona na obu końcach z rurkami; Rurkę wejściową podłączono z zanurzoną pompą akwariową (Atman, model 102, Guangdong, Chiny), która regulowała przepływ wejściowy po 8 l/min, naśladując typowe stawki w regularnych systemach GW Garden Garden Systems. Innymi słowy, każda próbka leczonych GW była narażona na ten sam czas kontaktu, chociaż jakość leczonych GW była zupełnie inna, a zatem może istnieć duża zmienność wymaganej dawki chloru. Próbki chlorowane zebrano z rurki wylotowej.
2.3.2. Przepływowy reaktor UV
Reaktor UV o niskim ciśnieniu przepływu (UV6A, Watertec Inc., Panchiao Tajpei, Tajwan) z czasem uruchamiania od włączenia do maksymalnej intensywności 100 s zastosowano do napromieniowania próbek (ryc. 1B). Reaktor (objętość 43 ml) zawierał lampę rtęci o niskim ciśnieniu 4 W i wynosił 1.O średnicy 6 cm i 13.Długość 5 cm. Więcej szczegółów na temat reaktora UV można znaleźć w [25]. Lampa została włączona na co najmniej 120 s, po czym poddane obróbce próbki GW przepompowano przez reakttor za pomocą pompy perystaltycznej (Masterflex, Cole-Parmer Instrument CO., Chicago, IL, USA) przy prędkości przepływu 24 l/h. Do określenia rzeczywistej średniej dawki UV w reaktorze wynosi 44 mj/cm 2, z obliczoną intensywnością lampy wynoszącą 20 mj/cm 2, zastosowano aktynometrię chemiczną jodku iodatowego (szczegółowe informacje, patrz [25]).8 MW/cm 2 i średni czas przebywania 14 s.
2.4. Modele wielu regresji liniowej (MLR)
Wyniki eksperymentów wsadowych zastosowano do opracowania modeli MLR. Modele mają na celu przewidywanie logarytmicznej inaktywacji FC na podstawie parametrów jakości wody i zastosowanej dawki środka dezynfekującego (napromieniowanie chloru lub UV). Parametry jakości wody wybrane dla modelu (TSS, Bod5 a stężenia FC LOG w GW przed dezynfekcją) miało znacząco wpłynąć na prognozę modelu i współczynnik oznaczania (r 2). Opracowane modele zostały zatwierdzone w stosunku do wyników z próbek wody szarości na miejscu, które uzyskano z eksperymentów reaktora przepływowego. Wreszcie, modele zastosowano do zaproponowania współczynnika konwersji między chlorowaniem lub kolimowaną kolimatyzowaną konfiguracją laboratoryjną wiązki i wyniki eksperymentalnych reaktorów przepływu ciągłego.
3. Wyniki i dyskusja
3.1. Eksperymenty wsadowe
Traktowane próbki GW, zawierające różne BZT5 i stężenia TSS zostały zdezynfekowane przez napromieniowanie chloru lub UV. Aby rozróżnić efekt każdego parametru (TSS lub rozpuszczony BZT5) Po redukcji FC wyniki eksperymentów z dezynfekcją okresową (chlorowanie lub napromieniowanie UV) podzielono na dwie kategorie: (1) Zmiana stężenia TSS, zachowując jednocześnie BZT5 stężenie poniżej 10 mg/l i (2) zmiana BZT5 Stężenie przy jednoczesnym utrzymaniu stężenia TSS poniżej 10 mg/l. Te progi zostały wybrane zgodnie z rządem Izraela’S Regulacja dla ponownego użycia ścieków oczyszczonych nieograniczonych oczyszczonych w nawadnianiu [26]. Należy zauważyć, że zakres TSS i BOD5 Stężenia zastosowane w tym badaniu reprezentują stężenia stwierdzone w GW [27].
3.1.1. Chlorowanie
Zgodnie z oczekiwaniami obecność TSS i materii organicznej zmniejszyła wydajność chlorowania w usuwaniu FC i była bardziej wyraźna dla niższych zastosowanych początkowych stężeń chloru, takich jak 0.5 i 1 mg/l.
Zmniejszenie wydajności chlorowania było zwykle bardziej wyraźne, gdy stężenie TSS było zwiększone, a nie gdy BOD5 Stężenia były wyższe (ryc. 2). Ponadto negatywny wpływ TSS rozpoczął się nawet przy niskich stężeniach (5 Na inaktywacji FC zaobserwowano tylko wtedy, gdy jego stężenie było wyższe niż 50 mg/l. Wyniki te są zgodne z wcześniejszymi ustaleniami [12,13], które sugerowały, że coli w GW były związane z cząsteczkami i były przez nich osłonięte; Zatem były odporne na dezynfekcję, podczas gdy materia organiczna wpłynęła na zapotrzebowanie chloru (a tym samym resztkowe stężenie chloru), ale nie oporność bakteryjna.
3.1.2. Klimatyzowana wiązka
Wydajność dezynfekcji UV FC wzrosła wraz ze wzrostem dawki UV, ale negatywnie wpłynęła na obecność TSS i BZT5 (Rysunek 3). Oczekiwano to, biorąc pod uwagę, że te składniki są znane z wchłaniania i/lub rozproszenia światła, zmniejszając w ten sposób dawkę UV pochłoniętą przez bakterie [16 28,29,30]. Wyniki te są zgodne z [13], którzy zalecili filtrację przed dezynfekcją UV, w celu usunięcia cząstek, w celu bardziej wydajnej dezynfekcji.
Zwiększenie stężenia TSS zmniejszyło wydajność dezynfekcji UV bardziej niż zwiększenie BZT5 stężenie (ryc. 4). Zmniejszenie wydajności inaktywacji UV FC było bardziej wyraźne przy niższych dawkach UV (7.5 i 15 MJ/cm 2). Na 7.5 mj/cm 2, próg zmniejszenia wydajności inaktywacji FC wynosił 50 mg/l TSS, osiągając ~ 1 logarytmiczne zmniejszenie wydajności inaktywacji, gdy stężenie TSS wynosiło ~ 100 mg/l. Przy dawce UV 15 mJ/cm 2 Wpływ wysokiego TSS na usuwanie FC był niższy, a przy dawce UV 30 mJ/cm 2 nie zaobserwowano. Wyniki te są zgodne z wcześniejszymi ustaleniami [4], którzy stwierdzili, że zmniejszenie FC 4-logowych można osiągnąć przez napromieniowanie UV o niskim ciśnieniu, gdy stężenie TSS jest utrzymywane poniżej 60 mg/l. W przeciwieństwie do tego, przy najwyższej badanej dawce 30 mJ/cm 2, prawie 100% inaktywacji FC osiągnięto dla całego zakresu TSS i BOD5 Testowane stężenia.
Bod5 (rozpuszczone) wykazywał inny trend niż TSS, z inaktywacją FC ledwo zmieniającą się, gdy dawka UV wzrosła z 15 do 30 mJ/cm 2 . Prawie 100% inaktywacji FC osiągnięto dla całego zakresu BZT5 Testowane stężenia (zachowując TSS < 10 mg/L) for UV doses of 15 mJ/ cm 2 and higher. This indicates that TSS influence UV disinfection efficiency more than dissolved organic substances. These findings were demonstrated previously by [31] who suggested that adjusting UV absorption through the composition of organic extracellular polymeric substances does not have a significant effect on UV disinfection. Furthermore, Ref. [30] compared the levels of UV absorption of various constituents and determined that wastewater and surface water organic matter exhibit lower UV absorption than suspended solids.
3.2. Model wielokrotnej regresji liniowej (MLR)
Opracowano modele MLR w celu opisania związku między logu inaktywacją FC a TSS, BOD5, Stężenie LOG FC leczonych GW (przed dezynfekcją) i zmierzonego całkowitego resztkowego chloru (równanie (1)) lub stosowanej dawki UV (równanie (2)).
FCInaktywacja = β1· [Bod5] + β2· [TSS]+ β3· [Log FC RAW]+ β4· [Chlor resztkowy]
FCInaktywacja = β5· [Bod5]+ β6· [TSS]+ β7· [Log FC RAW]+ β8· [Dawka UV]
gdzie fcInaktywacja jest w log (cfu/100 ml); Bod5, TSS i resztkowy chlor wynosi Mg/L; Log FC RAW jest w log (CFU/100 ml); Dawka UV w MJ/CM 2 i β1–Β8 Czy współczynniki szacują zmienne objaśniające (Tabela 1).
Należy zauważyć, że badano bardziej złożone modele zawierające kombinacje zmiennych objaśniających (w tym interakcje między nimi). Ponieważ jednak nie zwiększały dopasowania modeli, najprostsze są prezentowane. Aby porównać wpływ różnych zmiennych objaśniających na wydajność dezynfekcji UV/chlorowania, test wielkości efektu, który jest stosowany do oceny zmiennych’ zastosowano wpływ na sugerowany model. W tym teście wartość p przekształcono w logworth (−log10(wartość p)), zakładając, że większe efekty prowadzą do bardziej znaczących wartości p i większych wartości logworth (Tabela 1).
Oba modele wskazały, że początkowe stężenie drobnoustrojowe było najważniejszym parametrem (mającym pozytywny efekt). W przypadku chlorowania po początkowym stężeniu drobnoustrojowym nastąpiło TSS, a następnie BZT5 stężenia; Oba spowodowały zmniejszenie inaktywacji FC (efekt negatywny). Wyniki te są zgodne z ustaloną teorią i wykazują negatywny wpływ TSS i BOD5 na dezynfekcję chloru. Najprawdopodobniej część BOD5 a TSS zwiększyło zapotrzebowanie na chlor podczas utleniania, zmniejszając w ten sposób stężenie aktywnego chloru w ściekach, a w konsekwencji obniżając inaktywację FC. Ponadto, jak wspomniano, TSS i BOD5 może wpływać na wydajność chlorowania poprzez zwiększenie oporności bakteryjnej z powodu stabilizacji błon komórkowych mikrobiologicznych [14] lub z powodu przyczepności bakteryjnej do zawieszonych ciał stałych [12,13].
Model MLR, uzyskany z wiązki kolimowanej UV, wskazuje, że wysokie początkowe stężenia mikrobiologiczne i wysokie dawki UV powodują zwiększenie inaktywacji FC, podczas gdy zwiększenie stężenia TSS powoduje zmniejszenie inaktywacji FC. W tym przypadku efekt rozpuszczonego BOD5 nie było znaczące (w badanym zakresie). Wyniki te są zgodne z ustaloną teorią i wykazują negatywny wpływ TSS na dezynfekcję UV, prawdopodobnie z powodu “Efekt ekranowania i cieniowania” cząstek [29].
3.3. Konfiguracje przepływowe i weryfikacja modelu
Stężenia FC, TSS i BOD5 Od wcześniej leczonych GW (11 systemów na miejscu) wahało się od 0–10 6 CFU/100 ml, 3.Odpowiednio 9–233 mg/l i 0–107 mg/l (Tabela 2). Analizowano również liczbę FC po dezynfekcji i porównano z prognozami modeli.
Modele MLR, opracowane na podstawie eksperymentów fazowych, zostały zweryfikowane w stosunku do wyników ciągłych konfiguracji dezynfekcji przepływu (komora chlorowania i reaktor UV) i okazały się istotne statystycznie (p < 0.0001), with R 2 = 0.60 and R 2 = 0.84 for the chlorination and UV irradiation, respectively (Figure 5b,d). Although the quality of the treated GW from the two phases was quite different, as were the means of chlorination and UV irradiation, the models fitted well and explained most of the variability in the measured FC inactivation.
Korelacja chlorowania sugeruje, że możliwe byłoby przewidzieć wymagane resztkowe stężenie chloru potrzebne do reaktorów ciągłych (wspólne w systemach obróbki na pełnej skali), biorąc pod uwagę FC, BZT5 i stężenia TSS w leczonych GW (przed chlorowaniem) oraz wymagane końcowe stężenie FC po chlorowaniu, jak opisano w równaniu (3).
[r e q u i r e d r e s i d u a l c h l o r i n e] = f c i n a c t i v a t i o n – β 1 · [b o d 5] – β 2 · [t s] – β 3 · [log f c r a w] β 4
W razie potrzeby resztkowy chlor, BZT 5 a TSS są w mg/l; Inaktywacja FC jest w log (CFU/100 ml).
Kontrolowanie resztkowego stężenia chloru w reaktorze dezynfekcji przepływowej dla pewnej jakości GW wymagałoby manipulowania ilością chloru w reaktorze (e.G., liczba tabletek chloru) i/lub czas kontaktu (poprzez zmianę natężenia przepływu).
Jeśli chodzi o dezynfekcję UV, co ciekawe, różnica między modelem (na podstawie koliminowanych eksperymentów partii wiązki) stwierdzono przewidywanie wydajności inaktywacji FC i wyniki reaktora przepływowego (ryc. 5D). Ta różnica najprawdopodobniej wynikała z innego sposobu zastosowania promieniowania UV. W kolimowanej wiązce próbki były małe, dobrze wymieszane i bezpośrednio napromieniowane, podczas gdy w przepływu reaktora UV reżim przepływu był bardziej złożony (będąc częściowo dobrze wymieszanym i częściowo przepływem wtyczki [25]). Zatem nie wszystkie GW przechodzące przez reaktor otrzymały tę samą dawkę UV, co oznacza, że nie wszystkie FC obecne w GW były narażone na tę samą dawkę. Dla tej samej inaktywacji logarytmicznej podział zmierzonej dawki UV w reaktorze przepływowym (44 mj/cm 2 w tym badaniu) przez zaprojektowaną modelu dawkę UV (na podstawie wyników wiązki kolimowanej partii) spowodowało współczynnik korekty (CF) wynoszący 7.47 (std = 1.25). Ten czynnik przekształca dawkę UV wymaganą do pewnej inaktywacji FC w kolimowanych eksperymentach partii wiązki do dawki wymaganej przez reaktor przepływowy UV dla tej samej inaktywacji FC. Innymi słowy, aby osiągnąć tę samą inaktywację logarytmiczną dla wód o porównywalnej jakości (i.mi., TSS, BOD5 i stężenia FC przed dyskrożeniem), dawka UV wymagana w reaktorze przepływowym wynosi 7.47 razy wyższy niż dawka wymagana w kolimowanej wiązce. Ref. [32,33] Podają podobne różnice między wynikami eksperymentalnymi wiązki kolimowanej a wynikami reaktora przepływowego. Korzystając z modelu zmienionego przez CF, wymaganą dawkę UV w reaktorach przepływowych można ocenić na podstawie testów laboratoryjnych (równanie (4)).
[r e q u i r e d u v d o s e] = c f · f c i n a c t i v a t i o n – β 5 · [b o d 5] – β 6 · [t s] – β 7 · [log f c r a w] β 8
W razie potrzeby dawka UV jest w MJ/CM 2, inaktywacja FC jest w log (CFU/100 ml), BZT 5 a TSS są w mg/l; Log FC wiersz w dzienniku (CFU/100 ml); CF: 7.47 (Unitless).
4. Wnioski
W tym badaniu określono ilościowo wpływ jakości obróbki wód szarej (TSS, BZT5, i FC) zarówno na chlorowaniu, jak i efektywności dezynfekcji UV w konfiguracjach przepływu wsadowego i ciągłego.
Stwierdzono, że wydajność dezynfekcji chloru leczonych GW zmniejsza się w wyniku wzrostu TSS i BZT5 stężenia, w których efekt TSS był ciągły, począwszy od niskich stężeń, podczas gdy efekt BZT5 stał się znaczący tylko powyżej pewnego stężenia progowego. Eksperymenty z chlorowania wsadowym wykazały, że rozpuszczony materia organiczna wpływa na wydajność chlorowania znacznie mniejszą niż TSS, co odzwierciedla znacznie niższa wartość logwortha. Na podstawie wyników chlorowania wsadowego opracowano model MLR i z powodzeniem zweryfikowano w stosunku do wyników jednostki chlorowania przepływowego.
Wyniki eksperymentów dezynfekcji UV partii sugerują, że wydajność dezynfekcji UV leczonych GW zmniejsza się w wyniku zwiększenia stężenia TSS poza wartością progową 50 mg/l. Jednak wraz ze wzrostem stosowanej dawki UV wpływ TSS spadł. Wpływ rozpuszczonego BOD5 Stwierdzono, że podczas wydajności dezynfekcji UV jest nieistotna (w badanym zakresie stężenia).
Podobnie, w oparciu o eksperymenty z dezynfekcją UV partii, opracowano model MLR i został zweryfikowany w stosunku do wyników leczonych GW, który został zdezynfekowany przez przepływowy reaktor UV. Korzystając z tych dwóch modeli, można ocenić dawkę UV lub resztkowe stężenie chloru wymagane w reaktorach przepływowych na podstawie wyników partii. Takie podejście jest cenne nie tylko z operacyjnego punktu widzenia, ale także z perspektywy badań.
Materiały uzupełniające
Poniżej są dostępne online pod adresem https: // www.MDPI.COM/2073-4441/13/2/214/S1, Rysunek S1: Schemat systemu obróbki GW skonstruowanego przepływu pionowego (RVFCW) (po Alfiya i in., 2013); Rysunek S2: System wiązki kolimowanego UV trojanu z wyłączeniem migawki.
Autorskie Wkłady
Konceptualizacja, pozyskiwanie finansowania, metodologia, nadzór, przegląd i edycja: A.G. i e.F. Metodologia, Kuracja danych walidacyjnych, pisanie: D.F.C. i y.A. Wizualizacja, pisanie – przeciąg oryginalny, administracja projektu: y.G. Wszyscy autorzy przeczytali i zgodzili się na opublikowaną wersję manuskryptu.
Finansowanie
Badania zostały sfinansowane przez ZUK Maccabi Research Fund.
Oświadczenie instytucjonalne Radę Review
Nie dotyczy.
Oświadczenie o świadomej zgody
Nie dotyczy.
Instrukcja dostępności danych
Dane są zawarte w artykule lub materiały uzupełniającym.
Konflikt interesów
Autorzy nie deklarują konfliktu interesów. Funders nie odgrywali żadnej roli w projektowaniu badania; W gromadzeniu analizy lub interpretacji danych; w pisaniu manuskryptu lub w decyzji o opublikowaniu wyników.
Nomenklatura
| Bod5 | pięciodniowe biochemiczne zapotrzebowanie na tlen |
| FC | Kalili zbiorcze |
| GW | szara woda |
| Mlr | Wielokrotna regresja liniowa |
| RVFCW | recyrkulacja pionowego przepływu skonstruowanych podmokłych |
| TSS | Całkowite zawieszone substancje stałe |
| UV | Napromieniowanie ultrafioletowe |
| β1–Β8 | współczynniki |
Bibliografia
- Maimon, a.; Tal, a.; Friedler, e.; Gross, a. Bezpieczne ponowne użycie Greywater do nawadniania-krytyczny przegląd aktualnych wytycznych. Otaczać. Sci. Technol. 2010, 44, 3213–3220. [Google Scholar] [Crossref] [PubMed]
- Marzec, J.G.; Gual, m. Badania na temat chlorowania Greywater. Odsolenie 2009, 249, 317–322. [Google Scholar] [Crossref]
- Usepa (u.S. Agencja Ochrony Środowiska). Podręcznik systemów oczyszczania ścieków na miejscu; EPA 625-R-00-008, Office of Water; U.S. Agencja Ochrony Środowiska: Waszyngton, DC, USA, 2002. [Google Scholar]
- Fenner, r.A.; Komvuschara, k. Nowy model kinetyczny do dezynfekcji ultrafioletowej Greywater. J. Otaczać. Eng. 2005, 131, 850–864. [Google Scholar] [Crossref]
- Ekeren, k.M.; Hodgson, ur.A.; Sharvelle, s.mi.; De Long, s.K. Badanie dezynfekcji patogenów i odrastania w prostym systemie recyklingu Graywater do spłukiwania toalet. Desalination Water Treat. 2016, 57, 26174–26186. [Google Scholar] [Crossref]
- Och, k.S.; Leong, J.Y.C.; Poh, s.mi.; Chong, m.N.; Von Lau, e. Przegląd problemów związanych z recyklingiem Greywater: Wyzwania i przyszłe perspektywy w Malezji. J. Czysty. Szturchać. 2018, 171, 17–29. [Google Scholar] [Crossref]
- Leverenz, godz.L.; Darby, J.; Tchobanoglous, g. Porównanie dostępnego w handlu chloru i ultrafioletowej jednostki dezynfekcji dla systemów ścieków na miejscu. Małe przepływy mag. 2007, 8, 11–21. [Google Scholar]
- Friedler, e.; Kovalio, r.; Ben-Zvi, a. Badanie porównawcze jakości drobnoustrojów leczenia szarości traktowanych przez trzy systemy uzdatniania na miejscu. Otaczać. Technol. 2006, 27, 653–663. [Google Scholar] [Crossref]
- Friedler, e.; Yardeni, a.; Gilboa, y.; Alfiya, y. Dezynfekcja ścieków szarości i potencjału odrastania wybranych bakterii. Water Sci. Technol. 2011, 63, 931–940. [Google Scholar] [Crossref]
- UsePA (Agencja Ochrony Środowiska Stanów Zjednoczonych). Podręcznik dezynfekcji ultrafioletowej dla końcowej długoterminowej 2 Zwiększona reguła oczyszczania wód powierzchniowych; EPA 815-R-06-007 Office of Water; Usepa: Waszyngton, DC, USA, 2006. [Google Scholar]
- Benami, m.; Gillor, o.; Gross, a. Kwestia oceny ilościowej patogenu w dezynfekowanej wody szarej. Sci. Całkowite środowisko. 2015, 506, 496–504. [Google Scholar] [Crossref]
- Winward, g.; Avery, L.; Stephenson, t.; Jefferson, ur. Dezynfekcja ultrafioletu (UV) szarej wody: efekty wielkości cząstek. Otaczać. Technol. 2008, 29, 235–244. [Google Scholar] [Crossref]
- Bohrerova, Z.; Linden, k.G. Ultrafiolet i dezynfekcja Mycobacterium w ściekach: Wpływ agregacji. Water Environ. Res. 2006, 78, 565–571. [Google Scholar] [Crossref] [PubMed]
- Virto, r.; Manas, str.; Alvarez, i.; Condon, s.; Raso, J. Uszkodzenie błony i inaktywacja drobnoustrojów przez chlor przy nieobecności i obecności substratu żądającego chloru. Appl. Otaczać. Mikrobiol. 2005, 71, 5022–5028. [Google Scholar] [Crossref] [PubMed] [zielona wersja]
- Onga, Z.C.; Asadsangabifardb, m.; Ismailb, z.; Tama, J.H.; Roushenasa, s. 1. Projektowanie kompaktowego i skutecznego systemu uzdatniania wody w Malezji. Desalination Water Treat. 2019, 146, 141–151. [Google Scholar] [Crossref]
- Christensen, J.; Linden, k.G. Jak cząsteczki wpływają na światło UV w dezynfekcji UV niefiltrowanej wody pitnej. J. Jestem. Water Works Assoc. 2003, 95, 179–189. [Google Scholar] [Crossref]
- Carré, e.; Pérot, J.; Jauzein, v.; Lopez-Ferber, m. Wpływ zawieszonych cząstek na dezynfekcję UV ścieków aktywowanej w celu rekultywacji. J. Proces wodny eng. 2018, 22, 87–93. [Google Scholar] [Crossref]
- Beck, s.mi.; Rodríguez, r.A.; Salveson, a.; Goel, n.; Rhodes, s.; Kehoe, str.; Linden, k.G. Metody dezynfekcji do leczenia niskiego TOC, jasnoszarza do Kalifornii tytuł 22 standardy ponownego użycia wody. J. Otaczać. Eng. 2013, 139, 1137–1145. [Google Scholar] [Crossref]
- Madge, ur.A.; Jensen, J.N. Dezynfekcja ultrafioletowa kału coli w kalifli w ściekach miejskich: Wpływ wielkości cząstek. Water Environ. Res. 2006, 78, 294–304. [Google Scholar] [Crossref]
- Gross, a.; Shmueli, o.; Ronen, Z.; Raveh, e. Recyklingowy przepływ pionowy zbudowany podmokłe podmokłe (RVFCW) – nowatorska metoda recyklingu szarości do nawadniania krajobrazu w małych społecznościach i gospodarstwach domowych. Chemosfera 2007, 66, 916–923. [Google Scholar] [Crossref]
- Alfiya, y.; Gross, a.; SKLARZ, m.; Friedler, e. Niezawodność systemów obróbki wody szarościowej w środowisku śródziemnomorskim i suchym-studium przypadku. Water Sci. Technol. 2013, 67, 1389–1395. [Google Scholar] [Crossref]
- Apha; Awwa; WEF. Standardowe metody badania wody i ścieków, 22. wydanie.; American Public Health Association, American Water Works Association, Water Environment Federation: Washington, DC, USA, 2012. [Google Scholar]
- WHO (Światowa Organizacja Zdrowia). Wytyczne dotyczące bezpiecznego stosowania ścieków, wydalania i szarości – Volume 1 i Vol. 4 – Expreta i Greywater wykorzystuje w polityce rolniczej i aspektach regulacyjnych; WHO: Genewa, Szwajcaria, 2006. [Google Scholar]
- Mamane, godz.; Linden, k.G. Dezynfekcja UV rdzennych zarodników aerobowych: implikacje dla walidacji reaktora UV w niefiltrowanych wodach. Res. 2004, 38, 2898–2906. [Google Scholar] [Crossref]
- Friedler, e.; Gilboa, y. Wydajność dezynfekcji UV i jakość drobnoustrojów ścieków szarości wzdłuż systemu ponownego użycia do spłukiwania toalet. Sci. Całkowite środowisko. 2010, 408, 2109–2117. [Google Scholar] [Crossref] [PubMed]
- INBAR, y. Nowe standardy do ponownego użycia ścieków oczyszczonych w Izraelu. W ocenie ryzyka ponownego użycia ścieków, podejmowaniu decyzji i bezpieczeństwa środowiska; Springer: Berlin/Heidelberg, Niemcy, 2007; pp. 291–296. [Google Scholar]
- Gross, a.; Maimon, a.; Alfiya, y.; Friedler, e. Greywater Reuse; CRC Press: New York, NY, USA, 2015. [Google Scholar]
- Crittenden, J.; Trussell, r.; Ręka, d.; Howe, k.; Tchobanoglous, g. Obróbka wody: zasady i projekt, wydanie 2.; John Wiley & Sons Inc.: Hoboken, NJ, USA, 2005. [Google Scholar]
- Mamane, godz. Wpływ cząstek na dezynfekcję UV na ścieki wody i ścieków: przegląd. Obrót silnika. Chem. Eng. 2008, 24, 65–157. [Google Scholar] [Crossref]
- Cantwell, r.mi.; Hofmann, r. Właściwości absorpcji ultrafioletowej zawieszonych cząstek stałych w nietraktowanych wodach powierzchniowych. Res. 2011, 45, 1322–1328. [Google Scholar] [Crossref] [PubMed]
- Scott, godz.mi.; Liss, s.N.; Farnood, r.R.; Allen, d.G. Dezynfekcja ultrafioletowa ścieków reaktora Sekwencjonowania: badanie właściwości fizykochemicznych kłaczków drobnoustrojów i wydajności dezynfekcji. J. Otaczać. Eng. Sci. 2005, 4, S65 – S74. [Google Scholar] [Crossref]
- Cabaj, a.; Sommer, r.; Schoenen, zm. Biodosymetria: Obliczenia modelu dla urządzeń dezynfekcyjnych wody UV w odniesieniu do rozkładów dawki. Res. 1996, 30, 1003–1009. [Google Scholar] [Crossref]
- Kuo, J.; Chen, c.L.; Nellor, m. Standaryzowany protokół testowania wiązki kolimowanej do dezynfekcji ultrafioletowej wody/ścieków. J. Otaczać. Eng. 2003, 129, 774–779. [Google Scholar] [Crossref]

Rysunek 1. Jednostki przepływowe: (A) komora chlorowania; (B) Reaktor UV.
Rysunek 1. Jednostki przepływowe: (A) komora chlorowania; (B) Reaktor UV.

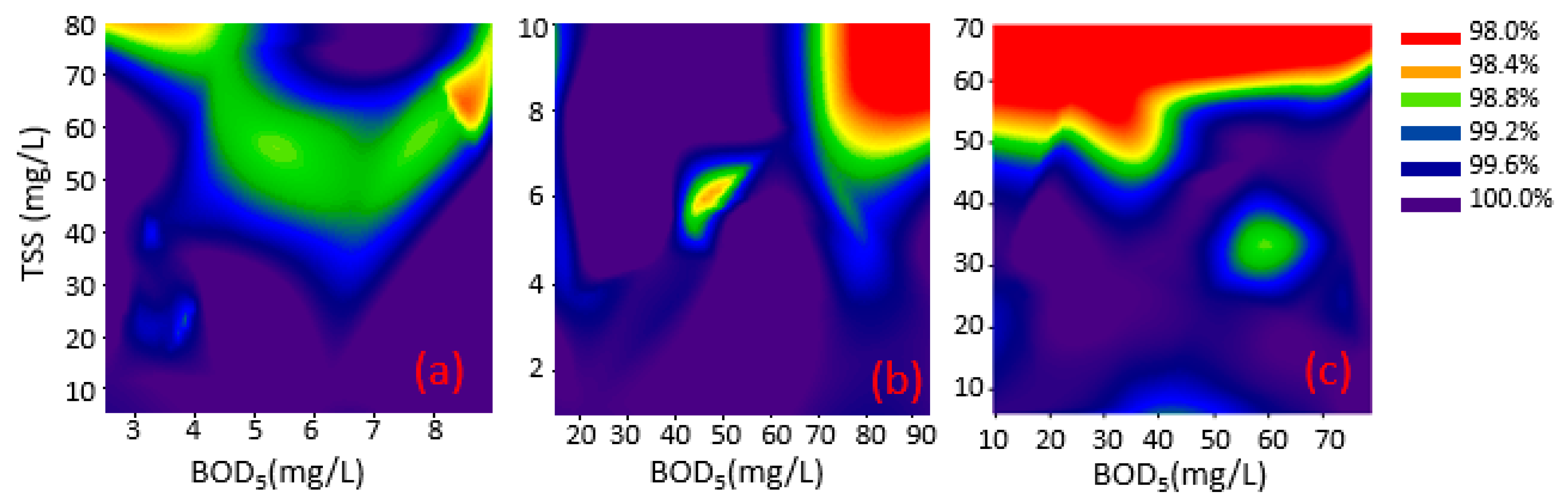
Rysunek 2. Wpływ TSS i rozpuszczonych BZT5 Stężenia w traktowanej wodzie szarości na inaktywacji coli w kale w ramach całkowitego resztkowego zakresu stężenia chloru 0.5–1.5 mg/l dla trzech różnych scenariuszy: wzrost TSS (A), wzrost BOD5 (B) i wzrost TSS i BOD5 (C). Kolory reprezentują procent inaktywacji z 96–100 % z przedziałem linii 0.5%.
Rysunek 2. Wpływ TSS i rozpuszczonych BZT5 Stężenia w traktowanej wodzie szarości na inaktywacji coli w kale w ramach całkowitego resztkowego zakresu stężenia chloru 0.5–1.5 mg/l dla trzech różnych scenariuszy: wzrost TSS (A), wzrost BOD5 (B) i wzrost TSS i BOD5 (C). Kolory reprezentują procent inaktywacji z 96–100 % z przedziałem linii 0.5%.

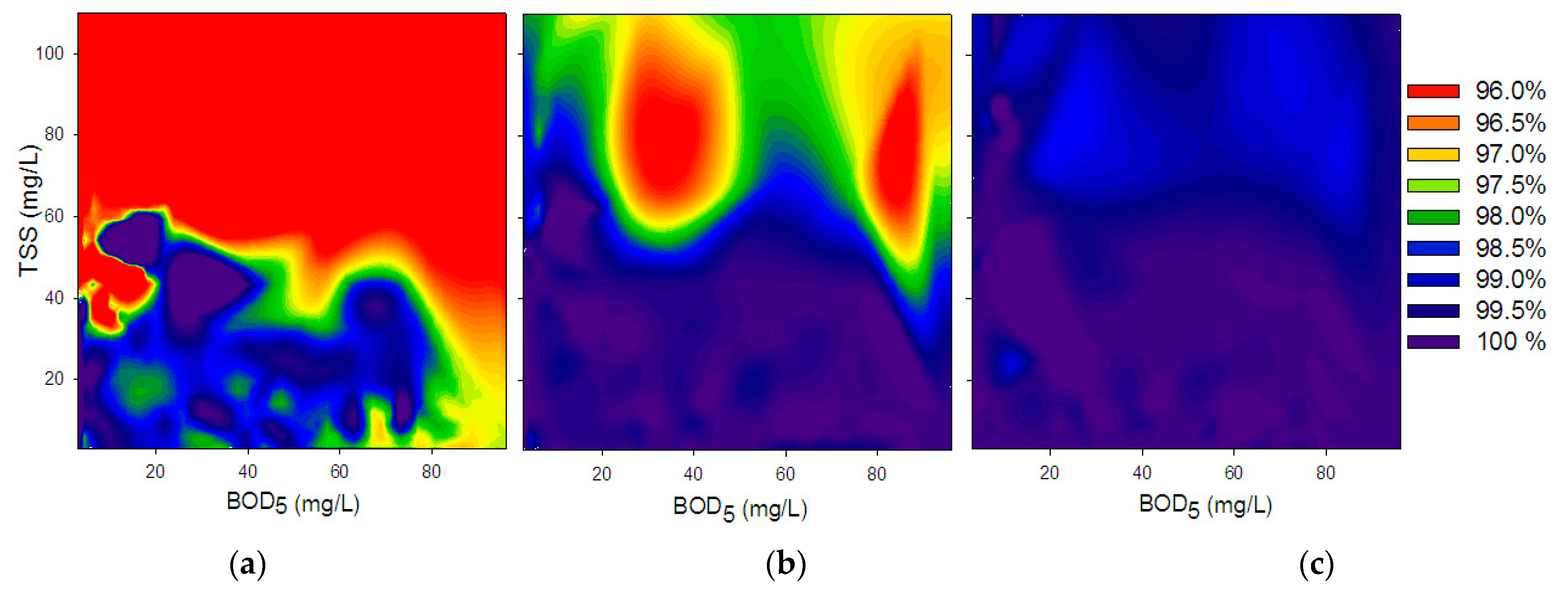
Rysunek 3. Wpływ TSS i rozpuszczonych BZT5 Stężenia w traktowanej wodzie szarej na inaktywacji coli w kale w trzech dawkach UV: (A) 7.5 (B) 15 i (C) 30 mj/cm 2 . Kolory reprezentują procent inaktywacji z 96–100% z przedziałem linii 0.5%.
Rysunek 3. Wpływ TSS i rozpuszczonych BZT5 Stężenia w traktowanej wodzie szarej na inaktywacji coli w kale w trzech dawkach UV: (A) 7.5 (B) 15 i (C) 30 mj/cm 2 . Kolory reprezentują procent inaktywacji z 96–100% z przedziałem linii 0.5%.

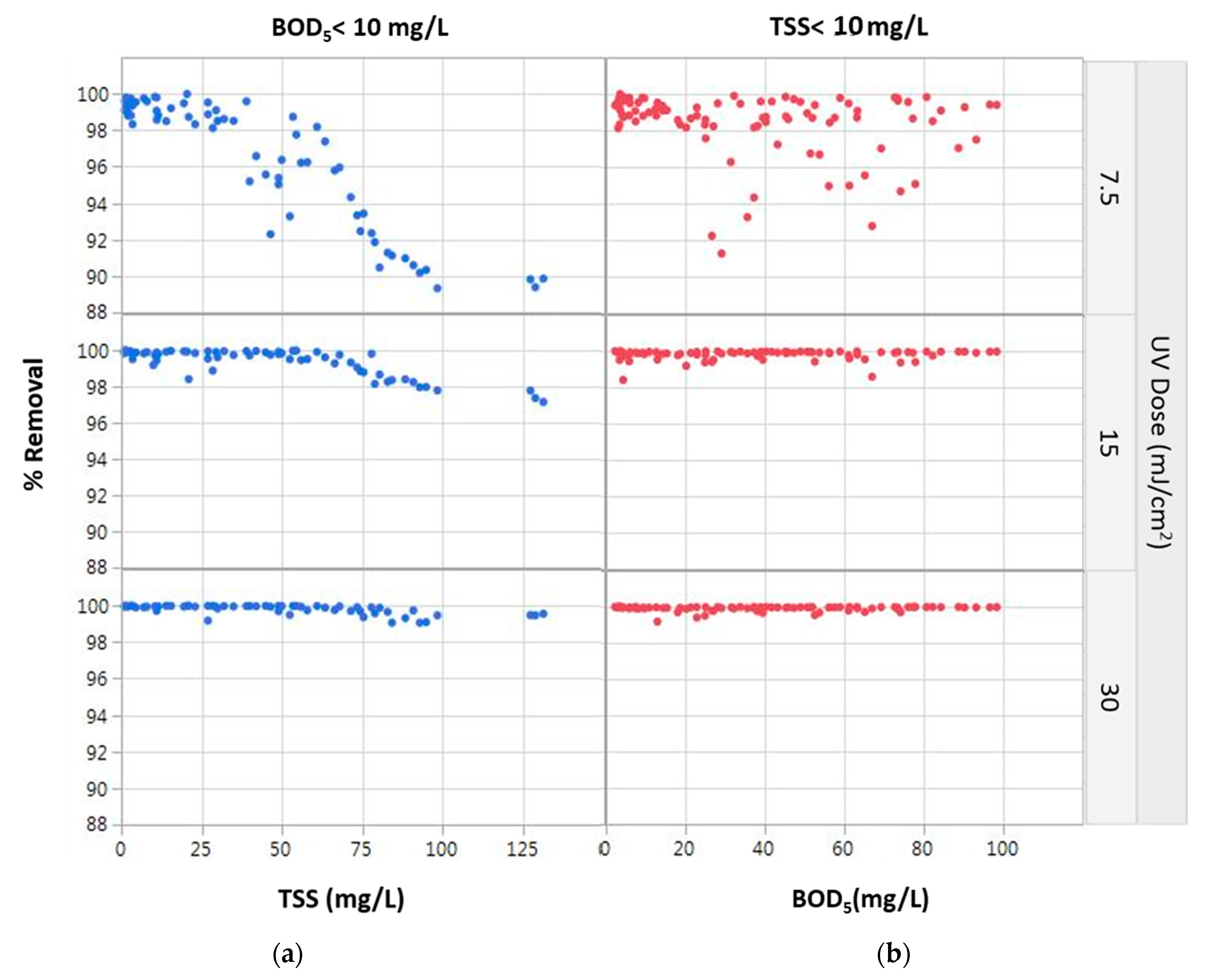
Rysunek 4. Wpływ TSS i rozpuszczonych BZT5 W przypadku inaktywacji FC w trzech dawkach UV: 7, 15 i 30 MJ/cm 2: (A) Na niskim bod5 koncentracja (b) przy niskim stężeniu TSS (
Rysunek 4. Wpływ TSS i rozpuszczonych BZT5 W przypadku inaktywacji FC w trzech dawkach UV: 7, 15 i 30 MJ/cm 2: (A) Na niskim bod5 koncentracja (b) przy niskim stężeniu TSS (

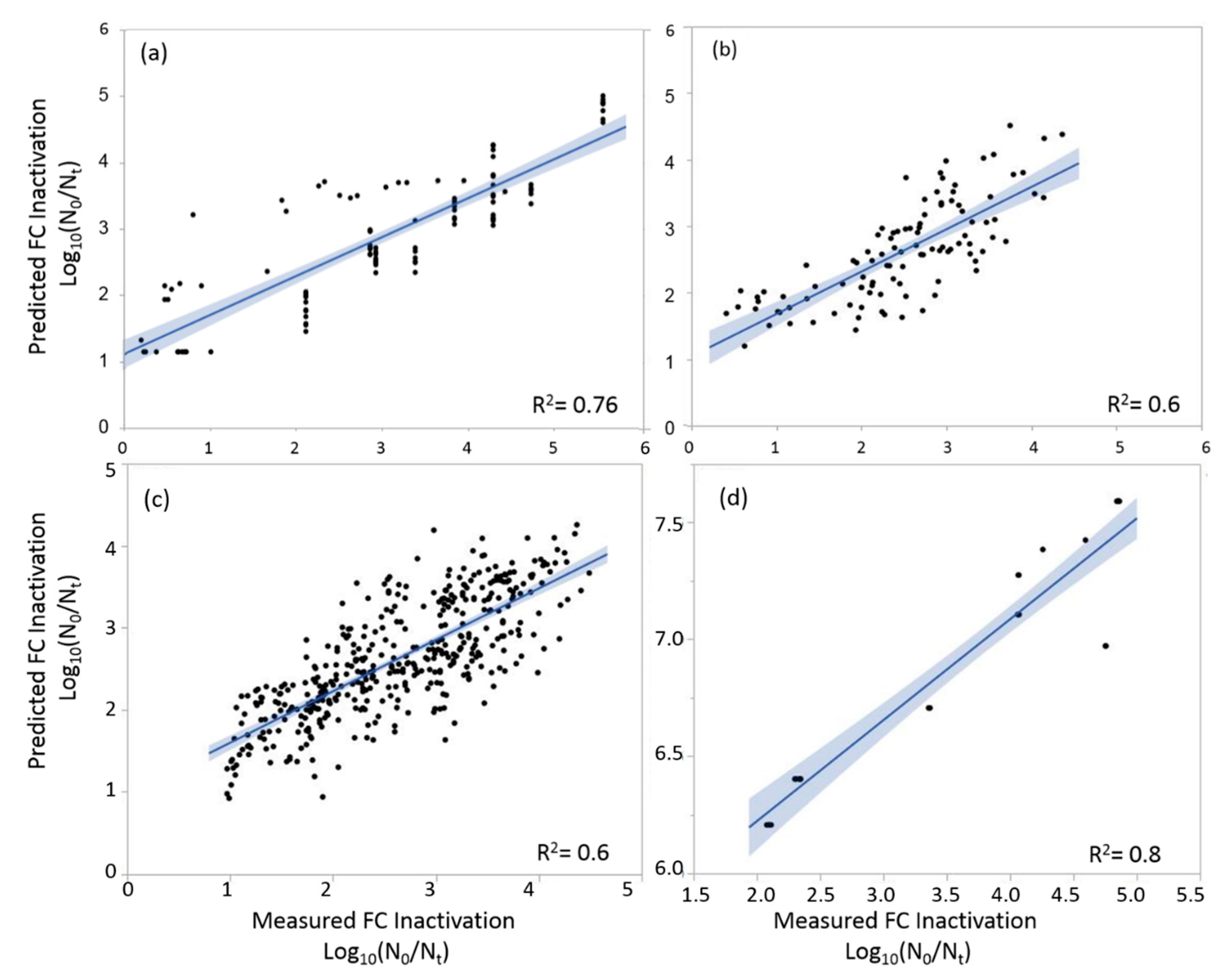
Rysunek 5. MLR – przewidywane vs. Zmierzona inaktywacja FC: (A) Konfiguracja chlorowania wsadowego (B) komora przepływowa chloru (C) Klimatyzowana wiązka UV i (D) Reaktor przepływowy UV.
Rysunek 5. MLR – przewidywane vs. Zmierzona inaktywacja FC: (A) Konfiguracja chlorowania wsadowego (B) komora przepływowa chloru (C) Klimatyzowana wiązka UV i (D) Reaktor przepływowy UV.

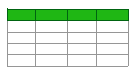
Tabela 1. Chlorowanie/dezynfekcja UV: Współczynniki modeli MLR.
Tabela 1. Chlorowanie/dezynfekcja UV: Współczynniki modeli MLR.
| Zmienna objaśniająca | Współczynnik | Oszacować | P -Wartość | Logworth | |
|---|---|---|---|---|---|
| Chlorowanie partii | Rozpuszczony bod5 (Mg/L) | β1 | −0.016 | 5.43 | |
| TSS (Mg/L) | β2 | −0.013 | 10.8 | ||
| Log FC RAW (Log (CFU/100 ml)) | β3 | 0.831 | 22.8 | ||
| Resztkowy chlor (mg/l) | β4 | 0.644 | 2.83 | ||
| Kolimowana wiązka promieniowania UV | Rozpuszczony bod5 (Mg/L) | β5 | 0.001 | 0.2211 * | 0.20 |
| TSS (Mg/L) | β6 | −0.012 | 23.0 | ||
| Log FC RAW (Log (CFU/100 ml)) | β7 | 0.495 | 43.5 | ||
| Dawka UV (MJ/CM 2) | β8 | 0.059 | 38.2 |
* Nie jest istotna statystycznie.

Tabela 2. Poziomy jakości próbek leczonych GW wcześniej, z 11 systemów obróbki na miejscu, które zastosowano w eksperymentach przepływowych. Każde miejsce próbkowano cztery razy (n = 44 próbki).
Tabela 2. Poziomy jakości próbek leczonych GW wcześniej, z 11 systemów obróbki na miejscu, które zastosowano w eksperymentach przepływowych. Każde miejsce próbkowano cztery razy (n = 44 próbki).
| Zakres | Przeciętny | Mediana | |
|---|---|---|---|
| TSS (Mg/L) | 3.9–233 | 38 | 15 |
| Rozpuszczony bod5 (Mg/L) | 0–107 | 41 | 37 |
| % Przenoszenie254 nm | 39–85 | 64 | 67 |
| Zmętnienie (NTU) | 1.47–512 | 87 | 18 |
| FC (CFU/100 ml) | 0–10 6 | 10 5 | 10 5 |
Wydawca’S Uwaga: MDPI pozostaje neutralne pod względem roszczeń jurysdykcyjnych w opublikowanych mapach i przynależnościach instytucjonalnych.
Udostępnij i cytuj
Styl MDPI i ACS
Friedler, e.; F. Chavez, d.; Alfiya, y.; Gilboa, y.; Gross, a. Wpływ zawieszonych ciał stałych i materii organicznej na efektywność dezynfekcji chloru i UV w Greywater. Woda 2021, 13, 214. https: // doi.Org/10.3390/W13020214
Styl AMA
Friedler E, F. Chavez D, Alfiya Y, Gilboa Y, Gross A. Wpływ zawieszonych ciał stałych i materii organicznej na efektywność dezynfekcji chloru i UV w Greywater. Woda. 2021; 13 (2): 214. https: // doi.Org/10.3390/W13020214
Styl Chicago/Turabian
Friedler, Eran, Diana F. Chavez, Yuval Alfiya, Yael Gilboa i Amit Gross. 2021. „Wpływ zawieszonych ciał stałych i materii organicznej na wydajność dezynfekcji chloru i UV w Greywater” Woda 13, nie. 2: 214. https: // doi.Org/10.3390/W13020214
Znajdź inne style
Zauważ, że od pierwszego wydania 2016 r. W tym czasopiśmie używa numerów artykułów zamiast numerów stron. Zobacz dalsze szczegóły tutaj.
Czy chlor zmniejsza BZT?
Sprawdź dostępu
Nasze systemy wykryły niezwykłą aktywność ruchu z Twojej sieci. Wypełnij tę Recaptcha, aby pokazać, że to ty składasz prośby, a nie robot. Jeśli masz problem z widzeniem lub wypełnieniem tego wyzwania, ta strona może pomóc. Jeśli nadal będziesz doświadczać problemów, możesz skontaktować się z wsparciem JSTOR.
Odniesienie blokowe: #E9CF1F44-F1C7-11ED-9C8B-464E53594559
Vid: #
IP: 65.108.68.174
Data i godzina: sobota, 13 maja 2023 19:54:04 GMT
© 2000- Ithaka. Wszelkie prawa zastrzeżone. JSTOR®, Logo JSTOR, JPass® i Ithaka® są zarejestrowanymi znakami towarowymi Ithaka.
Czy chlor zmniejsza BZT?
Sprawdź dostępu
Nasze systemy wykryły niezwykłą aktywność ruchu z Twojej sieci. Wypełnij tę Recaptcha, aby pokazać, że to ty składasz prośby, a nie robot. Jeśli masz problem z widzeniem lub wypełnieniem tego wyzwania, ta strona może pomóc. Jeśli nadal będziesz doświadczać problemów, możesz skontaktować się z wsparciem JSTOR.
Odniesienie do bloku: #EA036114-F1C7-11ED-9F09-7A6153727447
Vid: #
IP: 65.108.68.174
Data i godzina: sobota, 13 maja 2023 19:54:04 GMT
© 2000- Ithaka. Wszelkie prawa zastrzeżone. JSTOR®, Logo JSTOR, JPass® i Ithaka® są zarejestrowanymi znakami towarowymi Ithaka.
Wpływ dezynfekcji chloru na poziomy zapotrzebowania na biochemiczne
Ji Dai, Feng Jiang, Chii Shang, Kwok-Ming Chau, Yuet-kar TSE, Chi-Fai Lee, Guang-Hao Chen, Jingyun Fang, Liming Zhai; Wpływ dezynfekcji chloru na poziomy zapotrzebowania na biochemiczne. Water Sci Technol 1 lipca 2013 r.; 68 (2): 380–386. doi: https: // doi.Org/10.2166/WST.2013.257
Pobierz plik cytowania:
Tendencje odpowiedzi biochemicznego zapotrzebowania na tlen (BZT) i wytrzymałości organicznej po procesie chlorowania/deklorracji badano za pomocą 2-miesięcznego, 5-miesięcznego chemicznie wzmocnionego pierwotnego leczenia (CEPT) na miejscu monitorowania na miejscu oraz 2-miesięcznego badania laboratoryjnego. Wyniki monitorowania wykazały, że lepsze natychmiastowe mieszanie w punkcie iniekcji chloru zmniejszyło wpływ chlorowania/deklorowania na 5-dniowy poziom BZT. Wyniki badań laboratoryjnych wykazały, że chlorowanie nie zmieniło rozkładu wielkości cząstek, rozpuszczonego węgla organicznego ani zapotrzebowania na tlen chemiczny zawartości organicznej ścieków. Niemniej jednak chlorowanie/deklorowanie silnie wpłynęło na pomiar BZT, gdy nitryfikacja była hamowana przez zmianę szybkości bioaktywności/biodegradacji.


